ウィルスが私たちを健康にする
今回のタイトルは「ウィルスが私たちを健康にする」としました。
病原体であるウイルスが人にとって有用!?
まともじゃないように聞こえるかもしれないですが、果たしてそうでしょうか?
病気は、人を死に追いやることもありますが、病気になることでもっと恐ろしい病気に対する免疫を付けることもあります。
先日、「小児期にインフルエンザにかかることがその後の免疫力に影響する」
という記事にも書いたように、インフルエンザにかかることで免疫を得ることが出来るのであれば、その他のウイルスによる感染においても同じ事が言えるのではないでしょうか?
ウィルスに感染し、発症したということは体の調整するバランスが失われ、そのウイルスに対する抵抗力が弱まってしまった結果なわけです。
それが治ることにより、おそらくはバランスを崩してしまった、悪かった体内の環境を変化させ、また良いバランスに戻そうとしている体の反応なのかも知れません。
また前回には、このような記事も書きました。
「あなたの子どもを生涯健康でいさせたいのであればもっと汚れてもらおう」
免疫をつけることで、人は健康になっていく。
かつて敵であったとしても次には私たちの味方になってくれる。
そんな、お互いに利益のある共生社会こそが理想的な社会になるのではないでしょうか。
長い記事なので早速始めましょう。
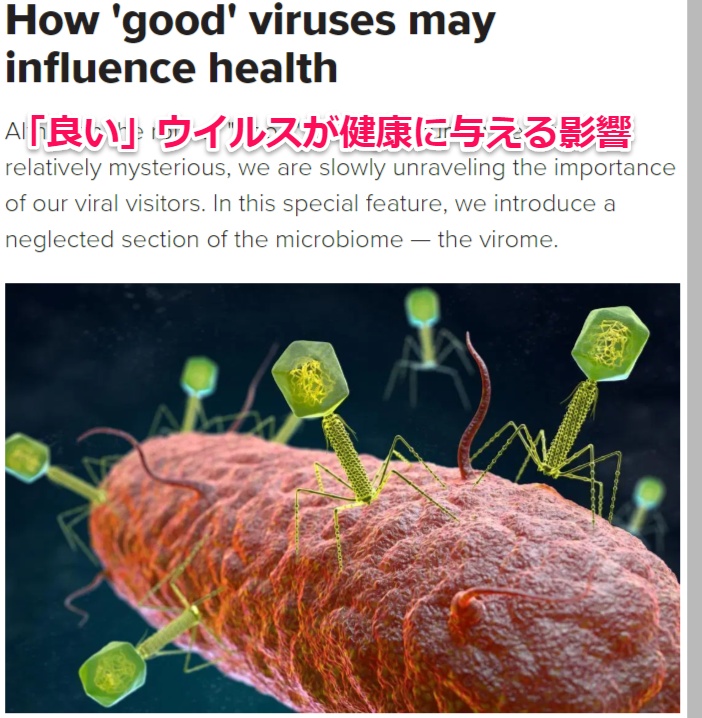
「良い」ウイルスが健康に与える影響
ここからです。
人間の健康における「良い」ウイルスの役割はいまだに不可解でありミステリアスだが、私たちはウイルスの訪問者の重要性を徐々にではあるが明らかにしつつある。この特別な特徴は、無視された微生物の部分、ビローム(腸内ウィルス)を紹介しよう。
健康と病気における細菌とマイクロバイオームの役割に対する研究は、医学研究の最前線だ。
私たちは、最近の調査結果によって提起された多くの質問に答えるため、遠い道のりを歩んでいるが、私たちの個人に「友好的な」微生物群、つまりマイクロバイオームなしでは繁栄できないことがはっきりと確立された。
しかし、医学はその根拠に基づいていません。その目は常に地平線を見つめ、遠方に隠されたものの形を見極めるために常に緊張しているようだ。
バクテリアと健康の間にある耐えられないほど複雑な相互作用を解明するのに苦労しているので、次の課題であるウイルスの役割についての出番を待たされている。
ビロームとは何か?
「マイクロバイオーム」という言葉を聞くと、すぐにバクテリアを思い浮かべるが、専門的には、マイクロバイオームは特定の環境におけるすべての微生物の総計だ。一部の科学者は、これらの微生物の遺伝物質の合計を指す用語として使用している。
そのため、バクテリアの他に、マイクロバイオームには、他の訪問者の中でもウイルス(ビローム)と菌類(マイコバイオーム)が含まれる。しかしこれまで、科学者はウイルスやマイコバイオームにほとんど注意を払っていなかった。
ウイルスは、人体のさまざまな生態学的なニッチ、特に鼻や口の内側や腸の内壁などの粘膜表面に生息している。
この特徴によって、ウイルスは腸内に集中している。そこはウイルスの占有が最も多い場所であり、最も調査されているからだ。
もちろん、ウイルスは天然痘、肝炎、HIV、狂犬病などの病気を引き起こすことで最も有名だ。緊急のウイルス性疾患に関連するためであり、この側面によって研究者の大半の時間を占めている。ただし、多くのウイルスにとっては、ヒトの細胞にはまったくといっていいほど関心を示さない。
バクテリオファージの紹介
科学者は、ビロームを「マイクロバイオームの最大かつ最も多様で、最も動的な部分」と考えており、腸内のウイルスの大部分はバクテリオファージだ。バクテリアがいるところはどこにでも、バクテリオファージが豊富にある。
他の研究者が説明するように、「ファージは地球上で最も豊富な生命体であり、事実上遍在しています。一部の淡水源には、1ミリリットルあたり最大100億個含まれる場合があります。」
バクテリオファージは細菌に感染し、その細胞機構を指揮し、それを使用して遺伝物質を複製する。
腸内細菌が健康と病気に影響を与えることは今や明らかになっているため、腸内細菌に感染するウイルスも重要な影響を与えることは驚くにはあたらない。
ファージ療法
1920年代から1950年代にかけて、科学者はバクテリア感染症の治療にバクテリオファージを使用できるかどうかを調査した。結局のところ、これらのウイルスは人間の病原体を破壊することに長けている。
科学者は、ファージ療法が効果的であり、重要なことに副作用がないことを発見した。
しかし、抗生物質が発見されてからは、ファージ療法は消えていった。なぜなら抗生物質は、比較的簡単に製造でき、広範囲の細菌種を殺すことができたからだ。
しかし、今日のハイテク能力と抗生物質に対する耐性菌の出現により、ファージ療法への関心が復活するかも知れない。
ファージ療法を魅力的なものにする1つの要因は、その特異性だ。多くの場合、抗生物質は広範囲の細菌種を一掃するが、(人にとって)「善良な」細菌が腸内に住んでいることもわかったため、(それさえも殺してしまうことになるので)これが理想的でないことは明らかだ。
一方、バクテリオファージは、同じ細菌種内の狭い範囲の株のみを標的とする。
さらに、ターゲットバクテリアがローカルエリアにある場合にのみ複製する。
これは、目的の細菌のみを攻撃し、感染を一掃するまで複製をし続けることを意味する。
一生の友人
バクテリオファージは、早い段階で人間への旅に出発する。ある研究では、新生児の最初の便である胎便を調べたところ、ウイルスは見つからなかった。しかし、生後わずか1週間の赤ちゃんの便には、1グラムにつき約1億個のウイルス粒子が含まれいて、そのほとんどがバクテリオファージだった。私たちのビロームは本当に生涯の仲間なのだ。
各ヒトには、バクテリオファージの明確な選択があり、これをまとめてファジオームと呼ぶ。ほぼ同じ食事をしている人は多くの類似点を共有するが、全体として、各個人のファジオームは大きく異なる。
共利共生から偏った共生へ*
前述のように、バクテリオファージはバクテリアを破壊します。ただし、状況によっては、バクテリオファージはバクテリアの集団に利益をもたらす可能性がある。腸内では、バクテリオファージは主にプロファージとして存在し、この段階で、遺伝子記号はバクテリアの遺伝子に組み込まれ、活性化されるとバクテリオファージを生産する準備が整う。
彼らの人生のこの時点で、バクテリオファージは細菌にとって有害ではなく、共生している。
バクテリアは遺伝物質を相互に交換できるため、プロファージの遺伝子記号も個々のバクテリア間で転送できる。
彼らは「抗生物質耐性、病原性、または異なる細菌種間の代謝経路に関連する遺伝子」を交換することができる。これはいくつかの細菌種に利益をもたらし、潜在的に彼らのニッチ(生息域)を広げることを可能にする。しかし、拡張は腸内のバクテリアの他のコロニーを犠牲にすることでもある。
「プロファージは宿主細菌と共生し、これらの細菌は私たちの体と共生します。したがって、ファージは宿主細菌の細胞がすぐに経験するものを超えて、人間のような多細胞生物に間接的に利益をもたらします。」
ストレスの発生時や宿主細菌が危険にさらされている場合など、プロファージがアクティブになるよう誘発されると、腸の微生物群集に広範な変化を引き起こす可能性がある。
無害なプロファージからいわゆる溶菌ファージへの移行は、細菌のコミュニティを一掃し、潜在的に「悪い」細菌にいくらかの空間を与えことになり、それらが空隙を満たすことができるようにする。
これは、コミュニティシャッフルと呼ばれ、微生物の不均衡である共生を引き起こす。
偏った共生から診断まで
不均衡な共生は、炎症性腸疾患、慢性疲労症候群、肥満、クロストリジウム・ディフィシル(C.デフ)感染、大腸炎など、さまざまな状態に関連している。
しかし、研究者たちは、これらの条件におけるバクテリオファージの役割についてまだ分かっていない。
これらの場合、他のメカニズムを介して不均衡な共生が起こる可能性がある。または、それが原因ではなく、状態によって起きている症状である可能性も考えられる。
研究者は、2型糖尿病、統合失調症、うつ病、不安、パーキンソン病など、驚くほど多様な病気の腸内細菌の変化を観察している。
なぜならバクテリオファージは、腸内のバクテリアよりも数が多く、複製するためにそれらに依存しており、変動の影響を受けるか、もしくは変動に関与している。
バクテリオファージは腸内の変化を促進していないかも知れない。加えなければならないのは、病気を促進しているのではなく、代わりに、バクテリオファージの集団は、腸内細菌の変化によって受動的に変化するだけなのかもしれない。
バクテリオファージの集団の衰退が健康と病気において重要であるかどうかは、調査が困難だ。しかし、それが病理学において大したことではないとしても、これらの変動を発見することには他の利点があるかもしれない。
例として、あるウイルスを診断マーカーとして使用する場合、たとえば科学者が、識別診断するのが難しいことで知られる、炎症性腸疾患を持つ人の腸内ウィルスに疾患特有の変化を特定した。
ウイルスのトラブル
細菌の研究は簡単では無く、それらは非常に小さく、直径は一般に0.4~10マイクロメートル(10マイクロメートルは100分の1ミリ)であり、ウイルスはさらに小さく、直径はわずか0.02~0.4マイクロメートルだ。
このような小さな尺度での作業の困難に加えて、ウイルスは他の課題ももたらす。
科学者が特定の集団にどの細菌種が存在するかを調べたい場合、遺伝子情報を抽出する。
これから、特定のコードストレッチを分離し、既存のデータベースに一致させる。最も一般的には、16S rRNA遺伝子を使用する。この特定の遺伝子は、ほぼすべての細菌種に見られ、進化の過程において比較的変化を起こしていない。
ただし、16S RNAの一部の領域は超可変と見なされ、これらの地域間の違いにより、研究者は種を識別することができる。
一方、ウイルスは種間で同等の遺伝子を共有しない。これは、比較的最近まで、ウイルスを研究することを不可能にしていたが、次世代シーケンシングの進歩は、徐々に障壁を打ち壊している。
この段階では、人間の健康におけるウイルスの役割は、病気におけるウイルスの役割ほど明確ではない。
そうは言っても、ウイルスが健康な体を維持する上で重要な役割を果たす可能性が高いと思われるので、研究技術の進歩がその完全な影響を理解できるようにるだろう。
抗生物質耐性の差し迫った懸念を考えると、おそらくバクテリオファージへの新たな関心は、医学のこの神秘的な要素により多くの時間を費やすことになるだろう。
それでも、マイクロバイオームの構成要素間の相互作用を理解することは、苦労して得られる情報だろう。
ある論文が説明しているように:
「腸内の微生物叢の組成は、人生のいくつかの段階で、あるいは同じ日の時間であっても同じではないのです。」
これは長い戦いになるだろう。
ここまでです。
※訳者注:「共利共生から偏った共生へ」
原文は、「From symbiosis to dysbiosis」となっており、”symbiosis”はそのまま共生と訳せるのですが、“dysbiosis”にあたる日本語が辞書では見つかりませんでした。専門用語のようで、ようやく以下に要約が見つかりましたので、参考までに文とリンク先を記載しておきます。
dysbiosis
腸内細菌叢を構成する細菌種や細菌数か゛減少することにより,細菌叢の多様性か゛低下した状態を示す.dysbiosisは主に抗生物質の投与や偏った食事,病原体感染といった外因性(後天性)と,遺伝的な素因による免疫異常なと゛の内因性(先天性)の原因によって引き起こされると考えられている.
理想に近い治療法
今回ファージ療法という抗生物質を使用しない治療方法があることを知りました。
しかも、重要なことは「副作用がない」ということです。
ファージ療法を魅力的なものにする1つの要因は、その特異性だ。多くの場合、抗生物質は広範囲の細菌種を一掃するが、(人にとって)「善良な」細菌が腸内に住んでいることもわかったため、(それさえも殺してしまうことになるので)これが理想的でないことは明らかだ。
このように、抗生物質は特定の細菌を殺すことはできず、私たちにとって無くてはならない良い細菌も殺してしまう事で、結局は腸内細菌叢の組成が変わってしまい、また別の病気を引き起こすといいう、負の連鎖となってしまいます。
抗生物質による腸内細菌叢の破壊についての記事は以前にも書いています。
「次々と明らかになってくる腸内細菌叢の破壊がもたらす原因不明の病気」
私たちが本当に健康で幸せに暮らせる社会は難しくなる一方のようです。